Effizientere spektroskopische Messungen durch in-situ Anwendungen
Eine erfolgreiche Tumorresektion wird durch ihre Vollständigkeit definiert. Bei heutigen Operationen wird dabei häufig die sogenannte Schnellschnittdiagnostik angewendet, bei der das Biopsat nach der Entnahme schockgefrostet, in dünne Scheiben geschnitten und mit Hämatoxylin-Eosin (HE) eingefärbt wird. Anschließend werden die Ränder des Tumors mikroskopisch begutachtet, wobei auch spektroskopische Untersuchungen möglich sind (z.B. hyperspektrale Bildgebung über FTIR-Spektrometer). Der komplette Untersuchungsprozess kann hierbei bis zu 30 Minuten in Anspruch nehmen und die Färberesultate sind im Vergleich zu histopathologischen Untersuchungen, bei denen die Proben zusätzlich in Formalin eingebettet werden, schlechter und weniger eindeutig zu bewerten. Deshalb wird in diesem Graduiertenkolleg ein multimodaler Ansatz verfolgt, bei dem mehrere Sensorprinzipien entwickelt und evaluiert werden, die eine Untersuchung in-situ, also direkt im Körper des Patienten und bereits direkt während der Operation ermöglichen sollen. Der multimodale Ansatz soll zudem die Zuverlässigkeit durch eine gegenseitige Absicherung der Sensoren gewährleisten.
Hauptprobleme beim Schnellschnittverfahren:
- Untersuchungsdauer von ca. 30 Minuten
- schlechte Färberesultate
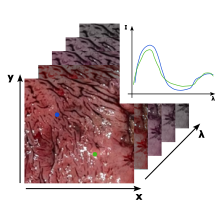
Der Ansatz in diesem Teilprojekt befasst sich mit der hyperspektralen Bildgebung im sichtbaren (VIS) und nahinfraroten (NIR) Spektralbereich. Hierbei wird das Gewebe mit polychromatischen Licht beleuchtet und die spektrale Antowort des Gewebes flächig detektiert. Anhand der so gewonnenen spektralen und räumlichen Informationen können verschiedene Gewebearten, anhand ihres Spektrums differenziert und klassifiziert werden.
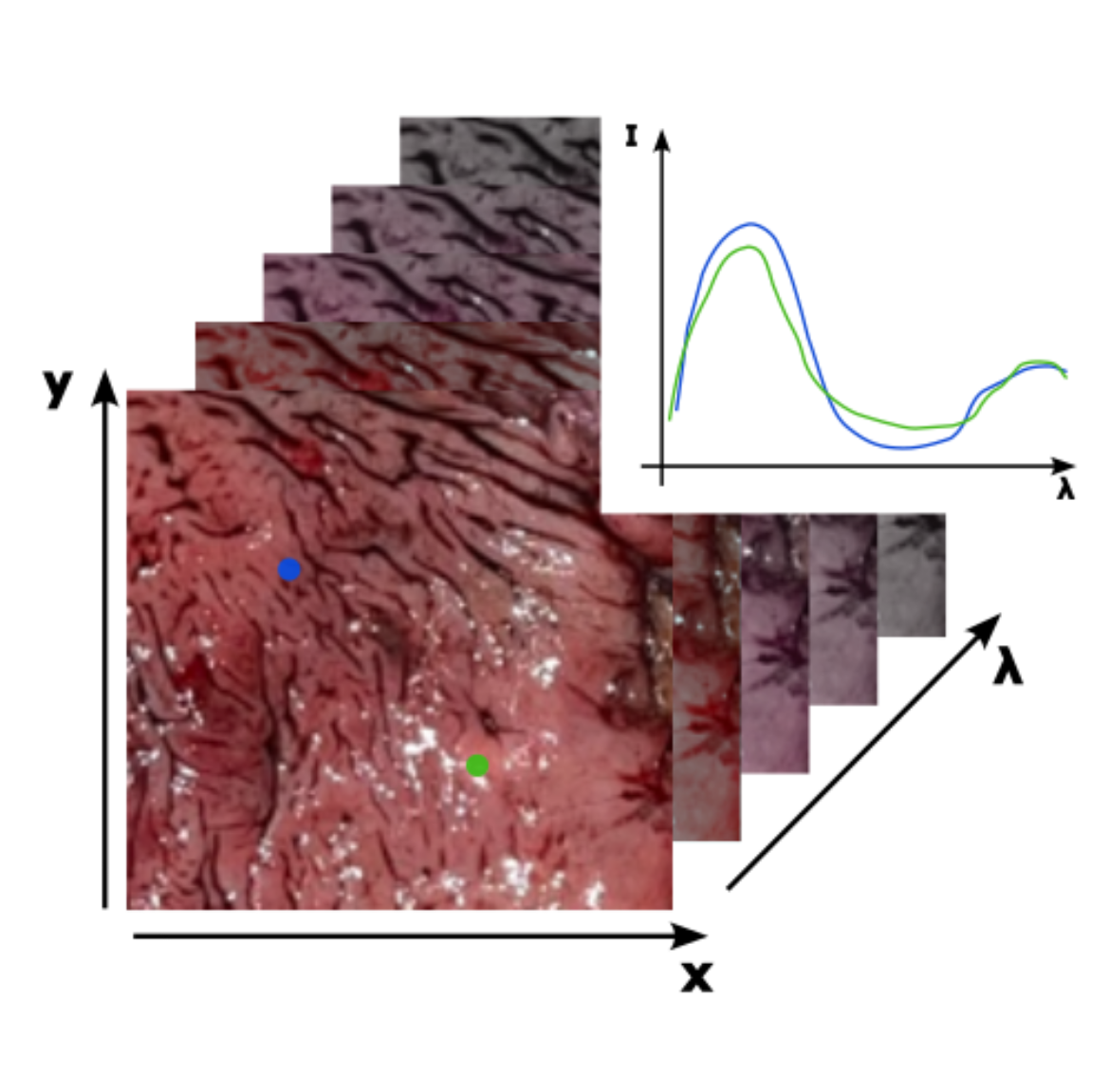
Optimierte Spektren
Die Ergebnisse der ersten Doktoranden-Kohorte hat gezeigt, dass ein stark begrenztes Spektrum im Infraroten zur Unterscheidung von malignem und benignem Gewebe ausreichen kann. Dies soll nun auf den VIS/NIR Spektralbereich übertragen und in Richtung potenterer Klassifizierungs- und Optimierungsalgorithmen weiter entwickelt werden.
Die Verwendung eines stark begrenzeten Spektrums bietet einige Vorteile:
- besseres Signal-Rausch-Verhältnis
- Reduktion auf die wesentlichen Daten
- kürzere Auswertedauer
Die erste Zielsetzung in diesem Teilprojekt liegt darin, dass geeignete Wellenlängen zur bestmöglichen Unterscheidung des Gewebes gefunden werden müssen. Dabei werden die folgenden unterschiedliche Ansätze verfolgt:
- Entwicklung eines Messaufbaus mit hoher räumlicher und spektraler Auflösung zur Datengenerierung
- Datenanalysen mit multivariaten statistischen Methoden (z.B. Principle Component Analyse)
- Einsatz neuronaler Netze
Integration des Sensors in ein Endoskop
Eine weitere Herausforderung liegt darin, einen miniaturisierten Sensor zu entwickeln, sodass dieser endoskopisch verwendet werden kann. Hierzu sind diverse hyperspektrale Snapshot Systeme denkbar, deren Umsetzung im Projektverlauf evaluiert werden muss. Eine zentrale Fragestellung dabei wird sein, wie die optimierten Spektren realisiert werden können.
Bearbeiter

Andrea Rüdinger
Doktorandin A2

Stephan Reichelt
Prof. Dr.-Ing.Betreuung A1, A2
- Profil-Seite
- +49 711 685 66074
- E-Mail schreiben
- Raum: 1.234

Tobias Haist
Dr.Betreuung A2
- Profil-Seite
- +49 711 685 66069
- E-Mail schreiben
- Raum: 1.253A